-
+86-825-7880081
-
Промышленная зона концентрированного развития, уезд Даин, провинция Сычуань
- sales8@shutaicn.com

Пожалуйста, оставьте нам сообщение
В 310 раз сильнее углекислого газа! Как сократить выбросы оксида азота — невидимого парникового убийцы?
2026-05-07
Когда речь заходит о парниковых газах, первым делом на ум приходит углекислый газ, однако мало кто обращает внимание на «невидимого убийцу» — оксид азота (N₂O). Являясь третьим по значимости парниковым газом, регулируемым Киотским протоколом, он обладает потенциалом глобального потепления в 310 раз выше, чем у CO₂, и в 24 раза выше, чем у CH₄. N₂O способен сохраняться в атмосфере в течение 150 лет, одновременно разрушая озоновый слой в стратосфере, что представляет угрозу для экологии и здоровья человека.
Промышленное производство (например, заводы по производству азотной и адипиновой кислот) является основным источником антропогенных выбросов N₂O. Вопрос о том, как эффективно сократить эти выбросы, стал важной темой в области защиты окружающей среды.
Ключ к успеху — в выборе правильного метода сокращения выбросов
Каталитическое разложение как оптимальное решение
В настоящее время существует несколько способов сокращения выбросов N₂O, таких как термическое разложение и каталитическое восстановление, однако все они имеют существенные недостатки: термическое разложение требует высоких температур (выше 600°C), что предъявляет чрезвычайно высокие требования к оборудованию; метод каталитического восстановления требует добавления восстановителей, что может привести к вторичному загрязнению. В то же время метод каталитического разложения можно назвать «оптимальным решением» — под воздействием катализатора N₂O напрямую преобразуется в нетоксичные азот и кислород. Этот метод не только требует гораздо более низких температур, чем термическое разложение, но и не вызывает вторичного загрязнения, являясь на сегодняшний день самой экономичной и экологически безопасной технологией сокращения выбросов N₂O.
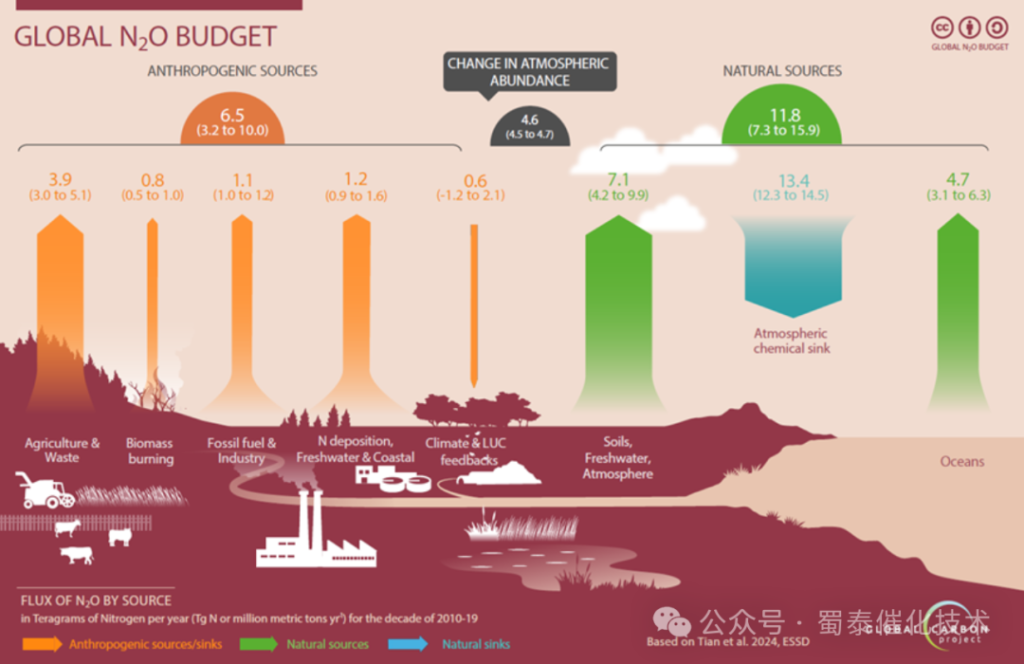
Однако в этом процессе есть свои «узкие места»: при разложении N₂O на активных центрах катализатора остается адсорбированный кислород, скорость десорбции которого напрямую определяет общую эффективность реакции. Ситуация осложняется тем, что примеси кислорода в промышленных отходящих газах подавляют реакцию разложения, причем степень влияния кислорода на разные катализаторы существенно различается.
Четыре основные группы катализаторов: преимущества и недостатки
1. Катализаторы на основе благородных металлов, представленные рутением (Ru), родием (Rh) и платиной (Pt). Их преимущество заключается в высокой низкотемпературной активности: например, катализатор Ru/TiO₂ обеспечивает полное разложение N₂O уже при 350°C, а катализатор Rh/Zn-Al₂O₃ при 275°C достигает степени конверсии N₂O в 98,7%. Однако благородные металлы дороги, а в процессе эксплуатации их частицы склонны к агломерации, что ведет к снижению активности. Поэтому их часто наносят на носители с большой удельной площадью поверхности для снижения расхода металла.
2. Катализаторы на основе оксидов металлов стали альтернативой для решения проблемы стоимости благородных металлов. Среди них выделяются оксиды со структурой шпинели. Например, кобальт-цериевый шпинельный катализатор, приготовленный с использованием KOH в качестве осадителя, полностью разлагает N₂O при 320°C; допирование щелочными металлами (K, Cs) позволяет дополнительно улучшить его окислительно-восстановительные свойства. Кроме того, свои преимущества имеют и другие оксиды металлов, такие как гидроталькиты и перовскиты: например, допированный калием катализатор Co-Mn-Al на основе гидроталькита способен стабильно работать в течение 112 дней, поддерживая конверсию N₂O на уровне около 90%.
3. Ионно-обменные цеолитные катализаторы обладают уникальной пористой структурой, однако их каркас склонен к разрушению в условиях высокотемпературного гидротермального воздействия. Исследователи оптимизируют их с помощью щелочной обработки и регулирования pH ионного обмена. Например, цеолит ZSM-5 с ионами железа после щелочной обработки не только демонстрирует повышенную активность, но и способен стабильно работать в течение 100 часов без потери эффективности.
4. Полупроводниковые фотокатализаторы являются перспективной технологией, позволяющей разлагать N₂O с использованием солнечной энергии, что сочетает в себе энергосбережение и экологичность. Текущие исследования сосредоточены на модификации TiO₂ и g-C₃N₄. Например, TiO₂, модифицированный церием (Ce), достигает степени конверсии N₂O в 82% при 18-часовом облучении, а композитный катализатор TiO₂/g-C₃N₄ показывает эффективность на 17% выше, чем одиночные компоненты. Тем не менее, все еще требуется решение проблем низкой эффективности использования солнечной энергии и быстрой рекомбинации фотогенерируемых пар электрон-дырка.
Будущие исследования: ориентация на низкие температуры, устойчивость к отравлению и высокую стабильность
На данном этапе каталитическое разложение N₂O все еще сталкивается со множеством проблем: большинству катализаторов требуется температура реакции выше 400°C, а водяной пар и оксиды серы в промышленных отходящих газах могут приводить к их отравлению. В будущем научные исследования будут сосредоточены на разработке катализаторов с высокой низкотемпературной активностью, сильной гидротермальной стабильностью и хорошей устойчивостью к отравлению. В то же время технологии фотокатализа требуют дальнейшего повышения коэффициента использования солнечной энергии и степени конверсии N₂O, чтобы обеспечить более «зеленые» решения для сокращения выбросов закиси азота.